|Cursos
2022| |Química de
11| Periodo 1
(Lección 01)
(Lección 02)
(Lección 03)
(Lección 04)
(Lección 05)
(Tarea 01)
(Tarea 02)
(Tarea 03)
(Tarea 04)
(Tarea 05)
(Encuesta
nota extra) (Tarea 06)
(Tarea 07)
(Tarea 08)
(Ave 1)
(Ave 2)
Periodo 2 (Lección 06)
(Tareas del
periodo 2) (Ave3)
(Lección 07)
(Lección 08)
Periodo 3 (Tareas del
periodo 03) (Lección 09)
(Ave
04) (abeja)
🧙 Conceptos clave
En
caso de no haber asistido a clase, transcriba la información presentada en los
siguientes enlaces a su cuaderno.
El barómetro
https://quimicadejoseleg-lamateria.blogspot.com/2022/01/barometro-manometro-aire-peso.html
El manómetro
Presión de vapor
https://quimicadejoselegcuantitativa.blogspot.com/2021/08/coligativas-presion-vapor.html
Propiedades de los gases
https://quimicadejoseleg-lamateria.blogspot.com/2021/06/propiedades-de-los-gases.html
🧙 Preguntas
Resuelva
los siguientes ejercicios
(3.1) Hallar el valor de la aceleración gravitacional, si la
presión atmosférica medida con un barómetro fue de 1.008 x 105 Pa y
la altura del barómetro de mercurio fue de 758 mmHg, y la densidad del mercurio
es de 1.35 x 104 kg/m3
(3.2) Cierto día, un barómetro de laboratorio indica que la
presión atmosférica es de 764.7 torr. Se coloca una muestra de gas en un matraz
unido a un manómetro de mercurio de extremo abierto y se usa una varilla de
medición para medir la altura del mercurio en los dos brazos del tubo en U. La
altura del mercurio en el brazo del extremo abierto es de 136.4 mm y la altura
del brazo en contacto con el gas en el matraz es de 90.0 mm. ¿Cuál es la
presión del gas en el matraz (a) en atmósferas, (b) en kilopascales?
(3.3) La presión de vapor de un líquido es la presión que
ejerce el vapor de ese líquido a una temperatura determinada. A 20°C se tienen
iguales cantidades de cuatro líquidos P,Q,R,S cada uno en un recipiente cerrado
conectado a un manómetro como se muestra en el siguiente dibujo.
De
acuerdo con la información anterior, es correcto afirmar que el líquido con
mayor presión de vapor es
A.
P B. Q C. R D. S
(3.4) El punto de ebullición normales (1 atm) de P es de 30°C y
de Q es 55°C. A 1 atm de presión y en recipientes diferentes, se deposita 1 ml
de cada una de las sustancias P y Q, y se espera hasta que alguna de las
sustancias se evapore completamente. La primera sustancia en hacerlo es P, lo
que indica que la presión de vapor de la sustancia
A.
Q es mayor que 1 atm B.
P es igual a la de la sustancia Q
C.
P es menor que 1 atm D.
P es mayor que la de la sustancia Q
La
presión de vapor es la fuerza que ejerce el gas en equilibrio sobre la superficie
del mismo líquido. Cuatro recipientes cerrados contienen líquidos diferentes
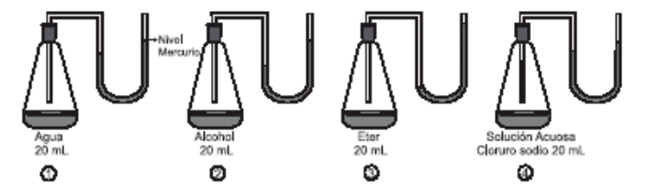
como se muestra en la siguiente figura
En
un experimento se destapan los cuatro recipientes durante determinado tiempo y
luego se tapan nuevamente
(3.5) Al finalizar el experimento el recipiente donde ha
quedado menos líquido es el que contiene
A.
agua B. éter C. alcohol D. solución cloruro de sodio
(3.6) Después de que se tapan los frascos se deja que se
equilibre la presión de vapor en cada uno. La presión de vapor final de cada
uno con respecto a la inicial será
A.
igual para los cuatro líquidos
B.
menor para los cuatro líquidos
C.
mayor para el éter y menor para los otros tres líquidos
D.
igual para el agua y el éter y menor para el alcohol y la solución de cloruro
de sodio
(3.7) Si se repite el experimento a una temperatura mayor es
probable que la presión de vapor en cada líquido sea
A.
mayor en todos los líquidos, porque estos se evaporan más rápido
B.
menor en todos los líquidos, porque la temperatura no influye en la presión de
vapor
C.
mayor en el éter y agua, porque son los líquidos menos volátiles
D.
menor en la solución de cloruro de sodio y el alcohol, porque son los líquidos
menos volátiles
La
tabla muestra las temperaturas de ebullición de cuatro sustancia líquidas a 1
atmósfera de presión.
(3.8) De
acuerdo con la información de la tabla, es correcto afirmar que a 25ºC el
líquido con mayor presión de vapor es
el
A. agua. B. éter etílico. C. metanol. D. benceno.
(3.9) De
acuerdo con la información de la tabla, es correcto afirmar que a 70ºC, las
sustancias que permanecen en estado líquido son
A. metanol y
agua. B. benceno y Éter etílico. C. benceno y agua. D. metanol y Éter etílico.


No hay comentarios:
Publicar un comentario